

El marcador más utilizado y mejor validado para el cáncer de páncreas es el CA 19-9. [1] El CA 50 es un nuevo marcador tumoral basado en un anticuerpo monoclonal (MAb) contra una línea celular de carcinoma colorrectal humano. [2] La detección de marcadores tumorales en suero (CA19-9, CEA, CA125 y CA242) favorece el diagnóstico precoz del cáncer de páncreas y la detección conjunta de marcadores tumorales ayuda a mejorar la eficacia del diagnóstico. [3]
Aunque se descubrió hace 30 años, el CA 19-9 sigue siendo el marcador sérico de referencia para los pacientes con cáncer de páncreas[1] El seguimiento mediante el CA 19-9 y el CA 50 es una forma sencilla y sensible de controlar la evolución postoperatoria de los pacientes con cáncer de páncreas, y puede ofrecer un plazo de varios meses para una recidiva en comparación con los métodos convencionales.
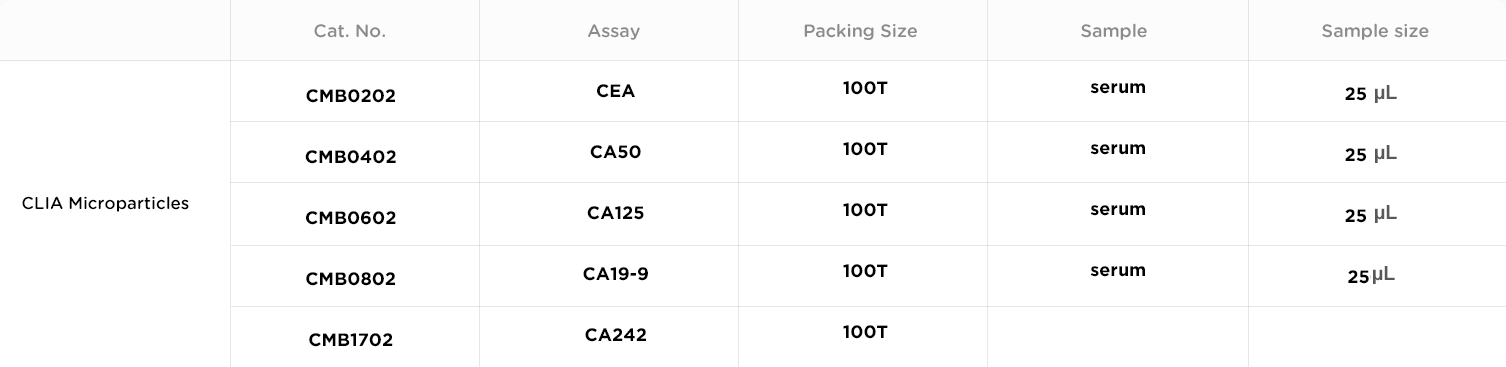
CA242 y CA19-9 tienen mejor rendimiento en el diagnóstico del cáncer de páncreas que el CEA. Además, el patrón de combinación paralela de CA19-9+CA242 podría considerarse de mejor valor diagnóstico para los pacientes con cáncer de páncreas[4].
CA50 is a glycolipid antigen that plays an important role in cell growth and differentiation. Subgroup analyses indicated that CA50 was the only tumor biomarker that was significantly correlated with long-term survival in CEA-normal CRC patients.[2]
El aumento de los niveles de los marcadores CA 19-9 y CA 125 en pacientes con anomalías patológicas pancreáticas suele indicar una naturaleza maligna de la lesión[5].
CA19-9, is inexpensive, convenient, and necessary for monitoring this disease.[6] Aunque el antígeno de carbohidratos 19-9 (CA19-9) es el biomarcador sérico más importante en el cáncer de páncreas, se está reconociendo gradualmente el valor diagnóstico y pronóstico del CEA.Además, los niveles elevados de CEA en suero están significativamente relacionados con el mal pronóstico de los pacientes con cáncer de páncreas. Por lo tanto, la medición del CEA sérico, como complemento vital del CA19-9, es barata, conveniente y necesaria para el seguimiento de esta enfermedad[6].
[1]M.J. Duffy, C. Sturgeon, R. Lamerz, A. Nicolini, O. Topolcan, V. Heinemann.Tumor markers in pancreatic cancer: a European Group on Tumor Markers (EGTM) status report. Annals of Oncology. VOLUME 21, ISSUE 3, P441-447, MARCH 01, 2010.
[2]CajHaglund,PenttiKuusela,HannuJalanko,Peter J. Roberts.Serum ca 50 as a tumor marker in pancreatic cancer: A comparison with CA 19-9.IJC International Journal of Cancer39(4):477-481. doi.org/10.1002/ijc.2910390412.
[3]Yu-Lei Gu 1, Chao Lan, Hui Pei, Shuang-Ning Yang, Yan-Fen Liu, Li-Li Xiao. Applicative Value of Serum CA19-9, CEA, CA125 and CA242 in Diagnosis and Prognosis for Patients with Pancreatic Cancer Treated by Concurrent Chemoradiotherapy. Asian Pac J Cancer Prev. 2015;16(15):6569-73. doi: 10.7314/apjcp.2015.16.15.6569.
[4]Yimin Zhang, Jun Yang, Hongjuan Li, Yihua Wu, Honghe Zhang, Wenhu Chen. Tumor markers CA19-9, CA242 and CEA in the diagnosis of pancreatic cancer: a meta-analysis. Int J Clin Exp Med 2015;8(7):11683-11691.
[5]GrzegorzĆwik, MD, PhD; GrzegorzWallner, MD, PhD; Tomasz Skoczylas, MD, PhD; et al.Cancer Antigens 19-9 and 125 in the Differential Diagnosis of Pancreatic Mass Lesions. Arch Surg. 2006;141(10):968-973. doi:10.1001/archsurg.141.10.968.
[6]QingcaiMeng, Si Shi, Chen Liang, Dingkong Liang, WenyanXu,Shunrong Ji, Bo Zhang, Quanxing Ni, JinXu,andXianjun Yu. Diagnostic and prognostic value of carcinoembryonic antigen in pancreatic cancer: a systematic review and meta-analysis. Onco Targets Ther. 2017; 10: 4591–4598.